Обеспечение качества и безопасности медицинской деятельности медицинской организации, ради чего, собственно, и должна быть создана и работать в каждой из них система внутреннего контроля, обязательно опирается на несколько базовых компонентов.
Внешние требования, исходящие из различных источников и относящиеся к медицинской деятельности и тем или иным её аспектам, конечно, составляют важнейшие компоненты фундамента системы внутреннего контроля медицинской организации.
Часть таких требований носит общеобязательный характер. Те же «Требования к организации и проведению внутреннего контроля качества и безопасности медицинской деятельности», утверждённые приказами Минздрава России от 7 июня 2019 года № 381н и от 31 июля 2020 года № 785н, обязательны для всех медицинских организаций. Положения уполномоченных органов исполнительной власти содержат требования, обязательные при осуществлении медицинской деятельности отдельных видов, связанных, например, с источниками ионизирующего излучения, медицинскими отходами, донорской кровью и её компонентами, и т.п. Требования порядков оказания медицинской помощи в их обязательной части могут иметь более или менее жёсткую привязку к профилю деятельности медицинской организации, но должны учитываться и соблюдаться всеми причастными к деятельности в сфере здравоохранения. И т.д.
Помимо обязательных, можно назвать ещё, по меньшей мере, три категории требований по их источникам. Прежде всего, это добровольные обязательства, принимаемые на себя хозяйствующими субъектами при осуществлении какой-либо деятельности в виде систематизированных сводов требований (систем стандартов) с целью получить официальное признание соответствия этим требованиям. В российском здравоохранении такие системы, позже получившие наименование систем добровольной сертификации, в 90-е годы развивались довольно активно. Помимо нашей «иркутской» системы (СДС «ЭкспертЗдравСервис»), в регионах использовались «алтайская», «кемеровская», «мурманская» и ряд других систем оценки соответствия в здравоохранении. На исходе первого десятилетия нового века, в силу глубокой трансформации нормативной правовой базы здравоохранения с упором на многосторонний контроль и надзор, эти разработки стали фактически невостребованными и были отложены до лучших времён, постепенно теряя актуальность. При этом, ожидаемо таяли и реальные возможности «отечественных производителей».
Сейчас мы наблюдаем второе пришествие добровольной сертификации, но уже с западными системами стандартов в сфере здравоохранения (JCI, HiMSS и др.) и локализованными международными «универсальными» стандартами типа ISO/ИСО. Также появляются российские системы стандартов, создаваемые на основе западных с учётом особенностей национальной системы здравоохранения (см, напр., Практические рекомендации Росздравнадзора к организации и проведению внутреннего контроля в медицинских организациях различного типа).
Последние продвигаются хоть и активно, но трудно. В этом месте нельзя обойти вниманием стремление «регулятора» сделать некоторые добровольные обязательства обязательными. Поиск «соуса» для «обязаловки» ещё ведётся. Насколько можно судить, он будет из разряда «национальных стандартов» – т.е., Практические рекомендации Росздравнадзора, скорее всего, получат статус условно добровольных требований, соблюдение которых обязательно при осуществлении того или иного вида деятельности.
Остальные системы стандартов либо «неподъёмные» и внедряются штучно на всю огромную страну, либо шире, но, в силу своего общего характера, без заметных улучшений собственно медицинской деятельности, слишком специфичной для подобных слабо дифференцированных решений.
И последняя категория – собственные управленческие потребности медицинских организаций, сформулированные самостоятельно либо заимствованные в той или иной системе стандартов и установленные в виде локальных требований. Удивительно, но без этой категории невозможно исполнить многие обязательные требования. В частности, лишённые конкретики федеральные «Требования к организации и проведению внутреннего контроля качества и безопасности медицинской деятельности» позволят создать или перестроить систему внутреннего контроля в медицинской организации, т.с., в структурном отношении, но не помогут добиться её эффективной работы. Для этого, потребуется её сначала наполнить фактическим содержанием. Причём, из разных источников, а там неизбежно возникнут проблемы интеграции.
К счастью, решаемые. Основные принципы систематизации требований при создании интегрированной системы управления качеством и внутреннего контроля были рассмотрены в работе Радомира Бошковича и Евгения Князева «О внедрении новых требований к организации и проведению внутреннего контроля в систему управления медицинской организации». Основополагающими идеями интеграции являются анализ информационных массивов требований, анализ, группировка и обеспечение составляющих деятельность процессов, опора на реальные потребности участвующих в этих процессах людей и выделение общих положений в интегрируемых системах. В ряду последних были названы такие универсальные составляющие, как документооборот, планирование, аудиты и контроль. В качестве напоминания, приведу рис.4 из той публикации.
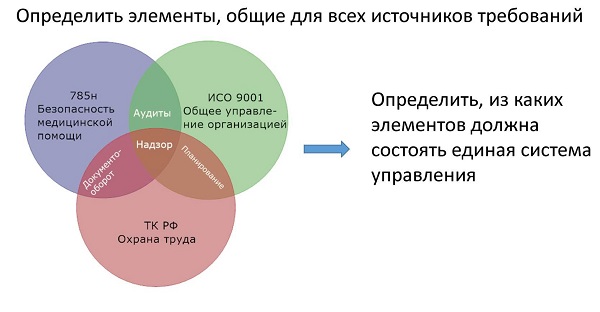
Рис.1(4). Примерная схема пересечения требований с выходом на интеграцию системы.
Конечно, можно найти и другие объединяющие универсальные или «сквозные» компоненты интегрируемых систем. По большому счёту, к ним относятся понятия, ценности, цели, принципы, подходы, методы, методики, инструменты и др. Проблемы тоже есть универсальные, резко обостряющихся в мульти- и мета-аналитических системах, на сведения из которых опирается система управления. Например, проблема измерения, проработанная мною ранее (см. публ. «Проблема измерения и Требования Минздрава по внутреннему контролю»), проблема стандартизации показателей, статью с рассмотрением которой никак не соберусь закончить, и т.д. Всё это необходимо учитывать, иначе единой системы управления не получится. Но как «переварить» колоссальный объём информации, что стоит за каждой внедряемой системой стандартов? Автоматизация нас спасёт?
В последнее время многие уповают на «цифру». Дескать, стоит загрузить туда, всё, что положено, и оно там само сделается в лучшем виде. Знай, потом, только выгружай, чтоб проверяющие были довольны. Этим надеждам не суждено оправдаться. Дело в том, что автоматизация хоть и расширяет возможности управления, однако сама управленческих проблем не решает. Если вы пойдёте, зачарованные открывающимися перспективами, от автоматизации, то будете бесконечно перекраивать и перестраивать информационные системы, которые будут стремиться работать сами на себя, ради заполнения чего-то, каких-то умопомрачительных баз и бесконечных полей. Вам придётся заставлять пользователей систем – т.е., и без того загруженных и перегруженных сотрудников, этим заниматься, упорно и бессмысленно.
Для того, чтобы получить в итоге рабочую систему управления, вы должны сначала найти нужные решения, увязать их между собой, и только затем можете автоматизировать. Автоматизация процессов в системе внутреннего контроля медицинской организации, таким образом, начинается не в компьютерах программистов, а в собственной модели интегрированной системы управления, исходя из содержания которой только и возможно грамотно ставить задачи разработчикам информационных систем.
С другой стороны, нет проектов, похожих один на другой, а индивидуальная разработка – это очень дорого. Тиражируемые решения позволяют значительно снижать стоимость продуктов для потребителей и соответственно повышать их доступность. Однако при этом возникает противоречие: необходимо учитывать не только массу качественно и не очень составленных требований, но и бесконечное разнообразие собственных управленческих потребностей медицинских организаций, что делает информационные системы слишком громоздкими, неповоротливыми, грубыми. В какой-то мере снизить остроту этой проблемы позволяет участие в разработке специалистов, обладающих опытом успешной реализации проектов по созданию интегрированных систем управления в медицинских организациях различного типа.
Проблема формирования универсальной технологической платформы, на которой можно было бы выстраивать автоматизированные системы управления качеством на основе различных систем стандартов и к тому же позволяющие медицинским организациями преследовать собственные управленческие цели, слишком сложна для сего дня. Её решение требует хорошей организации, упорного труда и значительных вложений, а также участия многих специалистов, обладающих разнородным опытом и при этом хорошо понимающих друг друга. Пока такого, чтоб наличествовали в достатке сразу все компоненты, не наблюдается.
Проблема усугубляется тем, что задачи автоматизации административных процессов системы внутреннего контроля и управления качеством во многих своих аспектах чужды идеологии медицинских информационных систем (МИС), где главное внимание уделяется тотальной регистрации событий, обработка которых и делает возможным извлечение преимуществ из информатизации. Конечно, идея аналогичным образом автоматизировать «качество» подкупает. Действительно, и здесь есть место формализованной регистрации событий и их обработке, и оно достаточно важное. Но главное, всё же, состоит в полноценной реализации принципов менеджмента качества, а это, так или иначе, люди – их знания, умения, стремления.
Пример. Вы можете захотеть завести в МИС контроль соблюдения эпидемиологической безопасности и, естественно, начнёте с обработки рук. Придумаете документ и станете автоматически контролировать его исполнение. Однако регистрация факта события «обработка рук» ничего не говорит о качестве обработки и никак не сказывается на частоте инфекционных осложнений. Начинается накручивание: добавить регистрацию времени начала и окончания обработки, расход моющего средства и воды, и т.д. Но и это всё ничего не сообщит о качестве. Чтобы полноценно автоматизировать только одну эту процедуру, потребуется проделать ещё кучу действий, зарегистрировать их, потратив на это много сил и времени, и обработать. Каких действий? А это ещё нужно придумать. К примеру, смывы отправлять на анализ после каждой обработки. Или устроить прямое видеонаблюдение процесса с анализатором на основе искусственного интеллекта. Смешно? Какие ещё будут предложения? У меня только одно: задаться вопросом, а действительно ли это надо?
В зрелой системе менеджмента качества люди сами будут делать, что и как нужно, потому что они сами так решили в результате проделанной работы – поиска информации, её анализа и обсуждения с коллегами. Они будут уметь это делать правильно и знать, почему именно так правильно, а также, что самое важное, они будут хотеть это делать правильно, помогать друг другу поддерживать форму и становиться лучше. Это я к тому, что не нужно сейчас бросаться набивать МИС ненужным функционалом, а лучше сосредоточить усилия на создании системы, помогающей культивировать всё лучшее в организации и изживать худшее. Для достижения улучшений важны не столько объективный формализованный результат оценки каждого движения в численном или, если угодно, дихотомическом «да/нет» выражении, сколько пояснения к нему эксперта или аудитора и его рекомендации по поводу того, что с этим желательно сделать.
Я уже не раз разбирал проблемы, возникающие при формировании системы оценочных критериев. Формализованная оценка помогает избежать произвола эксперта, но при условии разумной степени детализации и наличия внятной методики оценки. В решении любого вопроса вы можете дойти до конечных, неделимых параметров, и оценить их по факту, с помощью средств измерения и математических действий. Но чем глубже вы погружаетесь, тем больше времени и усилий потребует исследование, и тем большую погрешность вы накопите. Иногда такую, что конечный результат будет удивлять всякого разумного человека, компетентного в данной области. Нужно понимать, где идти до конца, а где остановиться и дать возможность эксперту оценить что-то на основе своих знаний и практического опыта.
Пытаясь автоматизировать задачи администрирования системы внутреннего контроля в МИС, вы неизбежно завязнете в неполноценной интерпретации имеющихся фактических данных и тщетных попытках дополнения их бесконечно недостающими сведениями. В итоге в лучшем случае вы получите имитационный модуль, требующий от многих людей регулярно тратить на него время, без заметных улучшений собственно качества и безопасности медицинской деятельности. Хуже того, вы сами приучите сотрудников к бездумному исполнению сочинённых вместе с разработчиком МИС и непонятных никому требований, что со временем закрепится в культуре организации и сделает реализацию принципов менеджмента качества в ней попросту невозможной.
Т.о., здравый подход к автоматизации заключается в настоящее время в разработке специализированного программного обеспечения, в котором были бы реализованы решения, выработанные предварительно в ходе создания интегрированной системы управления. Очевидно, это будет, в зависимости от реализации возможностей сквозного применения параметров в различных системах стандартов и их оценки в соответствии с предусмотренными ими оценочными методиками, мульти- или (лучше) мета-аналитической системой. И, конечно, это будет «конструктор», позволяющий маневрировать в системах оценочных критериев и показателей, создавать собственные структурированные наборы управленческих параметров, как из имеющихся в предустановленных базах требований*, так и полностью своих позиций, применять подходящие оценочные инструменты и шкалы, и т.д.
Принципиальным моментом является то, что медицинская организация должна иметь возможность совершенствовать свою деятельность и достигать поставленные перед собой цели в области качества с опорой на надёжные сведения, объективно и достоверно отражающие существующее положение вещей. Это предъявляет особые требования к функциональности и гибкости автоматизированной системы. Такая система должна также помогать управлять документами, планировать аудиты и другие мероприятия, назначать ответственных, устанавливать индикаторы процессов и отслеживать важнейшие параметры, организовывать обучение сотрудников, проводить аналитическую работу и т.д. Или, хотя бы, в развиваться в этих направлениях.
В то же время, в современных МИС содержится масса сведений, которые имеют значение для управления качеством или могут его обрести с помощью дополнительных аналитических инструментов. В перспективе, таких сведений будет становиться всё больше. Их можно и нужно использовать. Также будет полезным задействовать в управлении процессами возможности систем поддержки принятия решений, что особенно важно в отношении имеющего вероятностную природу основного «производственного» процесса медицинской деятельности – процесса оказания медицинской помощи пациентам. Традиционное управление документами, кадрами, знаниями, и т.д. также пересекается с управлением качеством. Так было всегда. В тех же СДС, о которых я говорил выше, обязательно оценивалась эффективность управления.
В последнее время необходимость интеграции проявилась очень чётко. Постепенно в ходе эксплуатации и совершенствования автоматизированных систем управления качеством будут проявляться области, в которых будет напрашиваться обмен данными с МИС. В ответ на растущие вместе с распространением идеологии СМК потребности медицинских организаций в эффективном управлении качеством станут развиваться стандарты обмена и появляться интеграционные модули различных МИС. Далёким относительно сегодняшней ситуации итогом прогресса будет т.н. «бесшовная» интеграция таких систем.
*В облачный сервис автоматизированного управления качеством MKT-Web (В.И. Калиниченко, компания «МедКомТех», г.Краснодар), разработку которого курируют эксперты нашей компании «ЭкспертЗдравСервис», в настоящее время загружены следующие системы стандартов и списки контрольных вопросов (проверочные листы):
- Чек-листы для проведения внутреннего контроля качества и безопасности медицинской деятельности:
1.1. Оценка готовности медицинской организации исполнить приказ Минздрава России от 31.07.2020 № 785н «Об утверждении Требований к организации и проведению внутреннего контроля качества и безопасности медицинской деятельности» (дорабатывается).
1.2. Предложения (Практические рекомендации) ФГБУ «ЦМиКЭЭ» Росздравнадзора: Стационар, 2017 (664 критерия).
1.3. Предложения (Практические рекомендации) ФГБУ «ЦМиКЭЭ» Росздравнадзора: Поликлиника, 2017 (753 критерия).
1.4. Предложения (Практические рекомендации) ФГБУ «ЦМиКЭЭ» Росздравнадзора: Поликлиника, 2017 (модернизирован 1 275 критериев) с возможностью ввода "Субкритериев".
1.5. Предложения (Практические рекомендации) ФГБУ «ЦМиКЭЭ» Росздравнадзора: Медицинская лаборатория, 2018 (230 критериев).
1.6. Предложения (Практические рекомендации) ФГБУ «ЦМиКЭЭ» Росздравнадзора: Медицинская лаборатория, 2018 (модернизирован 298 критериев) с возможностью ввода "Субкритериев".
1.7. Предложения (Практические рекомендации) ФГБУ «НИК» Росздравнадзора: Стоматология, 2019 (575 критериев).
- Чек-листы для оценки системы эпидемиологической безопасности:
2.1. «Оценка системы эпидемиологической безопасности в медицинской организации (стационар) в условиях пандемии COVID-19».
2.2. «Оценка системы эпидемиологической безопасности в медицинской организации (поликлиника) в условиях пандемии COVID-19».
2.3. «Оценка готовности больниц к заболеванию, вызванному коронавирусом COVID-19 // Центр по контролю и профилактике заболеваний США (CDC).
2.4. «Аудит эпидемиологической безопасности медицинских технологий. Аудит технологии обработки рук».
- Чек-листы для оценки системы по ГОСТ/ИСО:
3.1. ГОСТ 56906.2016 Бережливое производство. Организация рабочего пространства регистратуры 5S (25 критериев).
3.2. ГОСТ Р ИСО 9001-2015 (дорабатывается).
- Ведомственный контроль:
4.1. «Оценка соответствия органа исполнительной власти в сфере здравоохранения требованиям приказа Минздрава России от 31.07.2020 № 787н «Об утверждении Порядка организации и проведения ведомственного контроля качества и безопасности медицинской деятельности».
- Государственный контроль: чек-листы Федеральных органов государственного контроля (для самостоятельного проведения внутреннего контроля качества и безопасности медицинской деятельности так, как вас бы проверили специалисты Федеральных органов государственного контроля), в т.ч. списки контрольных вопросов (проверочные листы):
Росздравнадзора:
5.1. Приказ Росздравнадзора от 09.11.2017 № 9438. Приложения № 1, 10, 27, 28 (Государственный контроль за обращением лекарственных препаратов для медицинского применения в организации оптовой торговли лекарственными средствами).
5.2. Приказ Росздравнадзора от 09.11.2017 № 9438. Приложения № 2, 11, 19, 29, 37, 38, 39 (Государственный контроль за обращением лекарственных препаратов для медицинского применения в медицинской организации и иных организациях, имеющих лицензию на медицинскую деятельность).
5.3. Приказ Росздравнадзора от 09.11.2017 № 9438. Приложения № 3, 12, 20, 30 (Государственный контроль за обращением лекарственных препаратов для медицинского применения в аптеке готовых форм).
5.4. Приказ Росздравнадзора от 09.11.2017 № 9438. Приложения № 4, 13, 21, 31 (Государственный контроль за обращением лекарственных препаратов для медицинского применения в аптечном пункте).
5.5. Приказ Росздравнадзора от 09.11.2017 № 9438. Приложения № 5, 14, 22, 32 (Государственный контроль за обращением лекарственных препаратов для медицинского применения в аптечном киоске).
5.6. Приказ Росздравнадзора от 09.11.2017 № 9438. Приложения № 6, 15, 23, 33 (Государственный контроль за обращением для медицинского применения в аптеке производственной).
5.7. Приказ Росздравнадзора от 09.11.2017 № 9438. Приложения № 7, 16, 24, 34 (Государственный контроль за обращением лекарственных препаратов для медицинского применения в аптеке производственной с правом изготовления асептических ЛП).
5.8. Приказ Росздравнадзора от 09.11.2017 № 9438. Приложения № 8, 17, 25, 35 (Государственный контроль за обращением лекарственных препаратов для медицинского применения в медицинских организациях, расположенных в сельских населенных пунктах).
5.9. Приказ Росздравнадзора от 09.11.2017 № 9438. Приложения № 9, 18, 26, 36 (Государственный контроль за обращением лекарственных препаратов для медицинского применения индивидуальными предпринимателями).
5.10. Приказ Росздравнадзора от 20.12.2017 № 10449. Приложения №№ 1-7 (Государственный контроль за обращением медицинских изделий).
5.11. Приказ Росздравнадзора от 20.12.2017 № 10450. Приложения №№ 1-6 (Государственный контроль качества и безопасности медицинской деятельности).
Роспотребнадзора:
5.12. Приказ Роспотребнадзора от 18.09.2017 № 860 «Об утверждении форм проверочных листов (списков контрольных вопросов), используемых должностными лицами территориальных органов Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека при проведении плановых проверок в рамках осуществления федерального государственного санитарно-эпидемиологического надзора». Соблюдение обязательных требований на предприятиях (объектах) общественного питания (Приложение № 1).
МЧС России (Роспожнадзора):
5.13. Приказ МЧС России от 28.06.2018 № 261 «Об утверждении форм проверочных листов, используемых должностными лицами федерального государственного пожарного надзора МЧС России при проведении плановых проверок по контролю за соблюдением требований пожарной безопасности».
ФМБА России:
5.14. Приказ Федерального медико-биологического агентства от 10 июля 2019 г. № 136 «Об утверждении формы проверочного листа (списка контрольных вопросов), используемой должностными лицами Федерального медико-биологического агентства и его территориальных органов при проведении проверок соблюдения требований радиационной безопасности при обращении с радиоактивными веществами, радиоактивными материалами, радиационными источниками, радиоактивными отходами и промышленными отходами, содержащими радиоактивные вещества».
5.15. Приказ Федерального медико-биологического агентства от 21 октября 2020 г. № 307 «Об утверждении форм проверочных листов (списков контрольных вопросов), используемых Федеральным медико-биологическим агентством и его территориальными органами при проведении плановых проверок при осуществлении государственного контроля за обеспечением безопасности донорской крови и ее компонентов» (три чек-листа):
- Форма проверочного листа 1 (соблюдение организациями, осуществляющими деятельность по заготовке, хранению и транспортировке донорской крови и (или) ее компонентов, правил заготовки, хранения, транспортировки и клинического использования донорской крови и ее компонентов), согласно приложению № 1;
- Форма проверочного листа 2 (соблюдение организациями, осуществляющими деятельность по заготовке, хранению, транспортировке и клиническому использованию донорской крови и (или) ее компонентов, правил заготовки, хранения, транспортировки и клинического использования донорской крови и ее компонентов), согласно приложению № 2;
- Форма проверочного листа 3 (соблюдение организациями, осуществляющими деятельность по хранению, транспортировке и клиническому использованию донорской крови и (или) ее компонентов, правил заготовки, хранения, транспортировки и клинического использования донорской крови и ее компонентов), согласно приложению № 3.
Более подробную информацию об облачном сервисе автоматизированного управления качеством MKT-Web вы можете запросить и получить здесь.
Всегда ваши, команда Здрав.Биз и Андрей Таевский.








